همه چیز درباره وزیکولهای خارج سلولی
وزیکولهای خارج سلولی
وزیکولهای خارج سلولی (Extracellular vesicles)، اجسام کروی با غشا دولایه لیپیدی هستند که تقریبا توسط همه انواع سلولها به فضای خارج سلولی ترشح یا منتشر میشوند و نقش مهمی در ارتباط سلولی، بین سلولهای دور و نزدیک دارند. وزیکولهای خارج سلولی یا به اختصار EVs در پروسههای فیزیولوژیک و پاتولوژیک بسیاری از جمله ارتباطات بین سلولی، محافظت در برابر استرس و مرگ سلولی، اثرات ضد میکروبی، انعقاد خون، آنژیوژنز، تنظیم ایمنی، بدخیمی و التهاب نقش دارند. ترشح این وزیکولها به ویژه در شرایط فیزیولوژیک یا پاتولوژیک خاص، از این حیث که مانند محمولههایی مهم حامل اسرار و سیگنالهایی برای سلولهای دور و نزدیک هستند، مورد توجه قرار گرفتهاند.
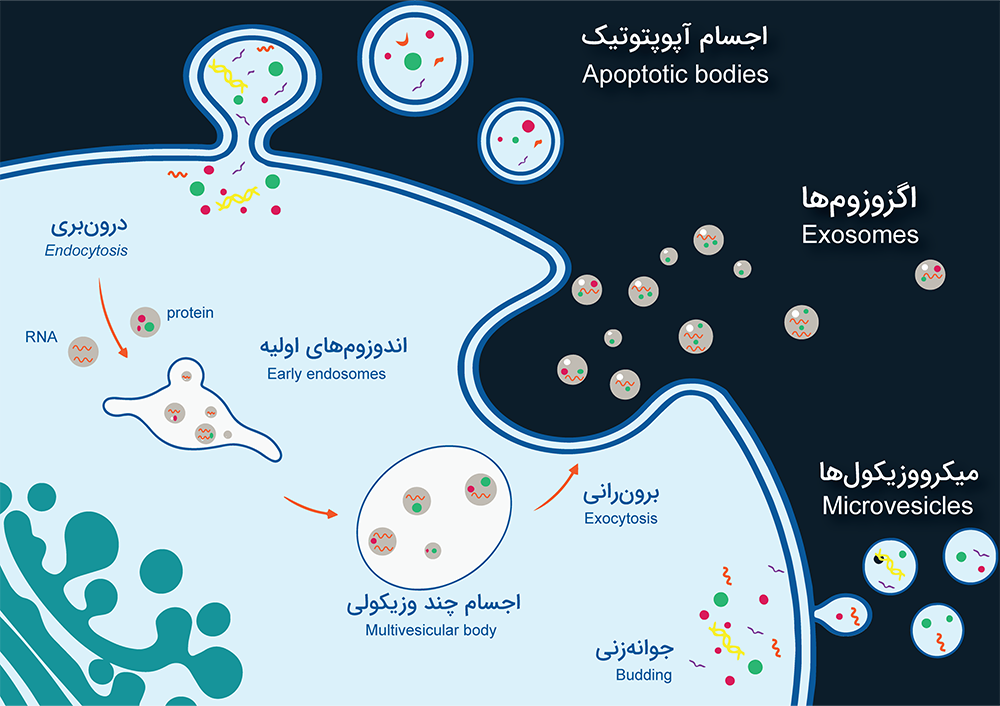
Evs به سه دسته عمده اگزوزومها (Exosome)، میکرووزیکولها (Microvesicles) و اجسام آپاپتوتیک (Apoptotic bodies) تقسیم میشوند، این سه دسته از نظر سایز، مسیر بیوژنز، آزادسازی(ترشح)، محتویات غشا، محمولهها و عملکرد با یکدیگر متفاوت هستند. اگزوزومها کوچکترین عضو این خانواده با قطر ۳۰-۱۰۰ نانومتر هستند، پس از آن میکرووزیکولها با ۱۰۰-۱۰۰۰ نانومتر و در نهایت اجسام آپاپتوتیک با ۱-۵ میکرومتر بزرگترین عضو این خانواده است.
اگزوزومها
اگزوزومها (Exosome) وزیکولهایی با اندازه نانو هستند که با ادغام اجسام چند وزیکولیMultivesicular body) و غشای پلاسمایی در مایعات بیولوژیک اطراف، آزاد میشوند. وجود اگزوزومها در فضای خارج سلولی در اواخر دهه 1980 شناسایی شد. با این حال، اگزوزومهای ترشح شده از سلولها در ابتدا بهعنوان ضایعات سلولی ناشی از آسیب سلولی یا محصولات جانبی هموستاز سلولی شناخته میشدند و تصور میشد تأثیر قابلتوجهی بر سلولهای مجاور ندارند. اخیراً نشان داده شده است این وزیکولهای خارج سلولی حاملهای کاربردی هستند که مجموعه پیچیدهای از پروتئینها، لیپیدها و نوکلئیک اسیدهایی را حمل میکنند و میتوانند این محمولهها را به سلولهای هدف نزدیک یا دورتر از محل آزادسازی که با آن مواجه میشوند برسانند. در نهایت ممکن است فعالیت سلولهای گیرنده را با ترکیبات زیستفعال خود تحت تاثیر قرار دهند. بنابراین، اگزوزومها حالت جدیدی از ارتباط بین سلولی را نشان میدهند، که ممکن است در بسیاری از فرآیندهای سلولی، مانند پاسخ ایمنی، انتقال سیگنال (signal transduction)، معرفی آنتی ژن نقش مهمی ایفا کند. تشکیل تنظیمشده اگزوزومها، ترکیب خاصی که با خود حمل میکنند، ویژگی هدفگیری اختصاصی سلولی (cell-targeting specifity) موجب اهمیت بیولوژیکی بسیار بالای اگزوزومها بهعنوان نشانگرهای زیستی تشخیصی (diagnostic biomarkers) غیرتهاجمی بالقوه و همچنین نانوحاملهای درمانی شده است. از آنجایی عملا تمام سلولهای یوکاریوتی میتوانند اگزوزوم آزاد کنند، بنابراین محمولههای آنها بسته به انواع سلولهای منشأ، نوع عملکرد سلولهای منشا و وضعیت آنها در زمان تولید اگزوزوم (به عنوان مثال تراریخته (transformed)، تمایزیافته (differentiated)، تحریکشده (stimulated) و تحت تنش (stressed)) بسیار با یکدیگر متفاوت باشد. بنابراین، اگزوزومها و محمولههای فعال بیولوژیکی آنها ممکن است اطلاعات پیشآگهی در طیف وسیعی از بیماریها، مانند التهابهای مزمن، بیماریهای قلبی عروقی و کلیوی، بیماریهای زوال عصبی (neurodegenerative) ، بیماریهای متابولیکی و تومورها ارائه دهند. تحقیقات اگزوزومی اکنون در مراحل ابتدایی خود است، درک عمیق اجزای درون سلولی و مکانیسمهای دخیل در تشکیل اگزوزوم و هدف قرار دادن سلولهای خاص، موضوعات داغ تحقیقاتی است که امید است در آینده فعالیتهای فیزیولوژیکی آنها را روشن کند. برای مشاهده کیت استخراج از اگزوزوم از محیط کشت اگزوسیب C و کیت استخراج اگزوزوم از سرم و مایعات بیولوژیک اگزوسیب S روی لینکها کلیک کنید.
میکرووزیکول (Microvesicle (MV))
میکرووزیکول که به نام میکروپارتیکل (microparticle) یا اکتوزوم (ectosome) هم شناخته میشود دستهای از وزیکولهای خارج سلولی هستند که از نظر ساختار مشابه اگزوزومها هستند و مانند آنها در شرایط فیزلوژیک و پاتولوژیک ترشح میشوند اما از اگزوزومها بزرگتر هستند و حدود ۱۰۰-۱۰۰۰ نانومتر قطر دارند، و برخلاف اگزوزومها طی مکانیزم جوانه زنی (budding) یا بیرونریزی غشای پلاسمایی (outward shedding) مستقیما از غشا آزاد میشوند، میکرووزیکولها از نظر سایز، ترکیبات لیپیدی، محتوا و مکانیزم تولید با اگزوزوم تفاوت دارند.
محتوای میکرووزیکولها به سلول مادری مولد، ریز محیط اطراف آن و محرکی که سبب آزادسازیش شده بستگی دارد اما به طور کلی محتوی میکرووزیکول شامل چربی، گیرندههای (receptor) بخشی از غشا که از آن آزاد شدهاند، کربوهیدرات، مواد ژنتیکی و پروتئین (مانند سایتوکاین، کموکاین، پروتئینهای دخیل در سیگنالینگ و مهاجرت و..) است، و به علت حمل این مواد بیواکتیو، قادر است فنوتایپ سلول گیرنده خود را تغییر دهد.
میکرووزیکولها هم در شرایط فیزیولوژیک خصوصا زمانی که سلول در حال رشد است، هم در شرایط پاتولوژیک و در اثر آسیب سلولی، هایپوکسی، استرس اکسیداتیو و محرکهای پیش التهابی تولید میشوند. میکرووزیکولها در اثر جوانه زدن غشا به سمت بیرون شکل گرفته و آزاد میشوند، اصلیترین موضوع در این فرایند، “خمیدگی غشا” میباشد که مسیرهای مولکولی مختلفی برای آن تعریف شده است.
بیشتر بخوانید
از معروفترین دلایل خمیدگی و جوانه زنی غشا، و تولید میکرووزیکولها، افزایش کلسیم درون سلولی است؛ در یک مکانیزم معروف برای تولید و رهاسازی میکرووزیکولها، با افزایش غلظت کلسیم سیتوزولیک، پروتئاز کالپین (calpain) (وابسته به کلسیم) اتصال پروتئینهای غشایی به اسکلت سلولی را قطع میکند، سپس ژل سولین با اتصال به فیلامنتهای اکتین (actin filaments) و شکستن شبکه پروتئینی آنها، سبب بازآرایی اسکلت سلولی و حبابزنی (blebbing) غشا پلاسمایی میشود.
به علت فرایند انتخابی جوانه زنی میکرووزیکول، ذخایر گیرندهها و محتویات آن کاملا مشابه سلول والد نیست، همچنین میدانیم در حالت استراحت، فسفاتیدیل سرین در لایه درونی غشا قرار دارد، میکرووزیکولها از بخشهایی از غشا (میکرودومینهایی) آزاد میشوند که گستره چربی (lipid rafts) یا دامینهای کاوئولا (caveolae domains) نام دارند، افزایش غلظت کلسیم درون سلولی، میتواند باعث فعال شدن آنزیمهای فلوپاز (floppase) که سبب حرکت لیپیدها به لایه بیرونی غشا میشود و آنزیم اسکرمبلاز (scramblase) که باعث حرکت لیپیدها به صورت دوطرفه در غشا میشود؛ گردد که در نهایت میتواند با قرار دادن فسفاتیدیل سرین در لایه خارجی، بار غشا میکرووزیکول منفی شود (البته این خصوصیت مطلق میکرووزیکلها نیست).
اجسام آپاپتوتیک (ApoBDs) آخرین وصیت سلول
ApoBDs گروهی از وزیکولهای خارج سلولی هستند که برخلاف اگزوزوم و میکرووزیکولها که از انواع سلولها مشتق میشوند تنها از سلولهای تحت آپاپتوز منشا میگیرند، ApoBDs به وضوح از اگزوزومها و میکرووزیکولها بزرگترند و قطری حدود ۵۰-۵۰۰۰ نانومتر دارند (اندازهای مشابه پلاکتها) و طی تغییرات مورفولوژیک سلول تحت آپاپتوز، تولید میشوند. حباب زنی (blebbing) غشا، که از مراحل شاخص تغییرات مورفولوژیک طی آپاپتوز است، شناخته شدهترین مکانیزم تولید اجسام آپاپتوتیک میباشد، اگرچه اخیرا دیده شده تغییرات غشا سلول طی آپاپتوز و تشکیل اجسام آپاپتوتیک منحصر به مدل حبابزنی نمیباشد.
اهمیت اجسام آپوپتوتیک
آپاپتوز یک فرایند شدیدا کنترل شده در موجودات پرسلولی است، تحقیقات نشان داده است هرگونه اختلال در روند آپاپتوز میتواند سبب بیماری گردد، پاکسازی کافی و به موقع بقایای سلول مرده یکی از جوانب اهمیت وجود آپاپتوتیک بادیها است، پاکسازی طی مکانیزم فاگوسیتوز اجزای سلول مرده(efferocytosis) توسط فاگوسیتها صورت میگیرد، هرگونه اختلالی در فرایند پاکسازی بقایای سلول مرده، میتواند سبب شناسایی اتوآنتی ژنها توسط سلولهای سیستم ایمنی و بروز بیماریهای خود ایمنی گردد. در این فرایند با تولید سیگنال “find me” توسط سلول در مراحل آغازین آپاپتوز شروع، و با سیگنال”Eat me” اجسام آپاپتوتیک تکمیل میشود.
افزون بر این، ApoBDs قادرند DNA سلول آپاپتوتیک را به به سلولهای مجاور (حتی اگر از یک تایپ نباشند) منتقل کرده و حتی در ژنوم آن¬ها الحاق کنند، این پدیده انتقال عرضی DNA (Horizontal transfer of DNA) نام دارد. خصوصیات انتقالی به بخشی از DNA مربوط است که توسط ApoBDs حمل می¬شود، برای مثال با انتقال انکوژنها امکان ایجاد تومور در سلول میزبان افزایش مییابد
همچنین ApoBD حاصل از Tcellهای آلوده به ویروس HIV، با انتشار اجزای ویروس به سلولهای اپیتلیال به انتشار ویروس کمک کنند، مشابه این رویداد در اجسام آپاپتوتیک مشتق از سلولهای آلوده به پریونها نیز رخ می¬دهد. بنابراین نوع محتویات منتقل شده، تعیین کننده نتیجه در سلول میزبان است.
لازم به ذکر است، برخلاف تصور رایج، تولید اگزوزوم و میکرووزیکول منحصر به سلول سالم نیست و سلول آپاپتوتیک نیز قادر به ترشح انواع وزیکولهای خارج سلولی میباشد، اگزوزومهای حاصل از سلول در حال آپاپتوز (ApoExos) از نوظهورترین موضوعات مورد مطالعه در زمینه آپاپتوز هستند و توجهات بسیاری را به خصوص در حوزه پاسخ ایمنی و التهاب به خود جلب کردهاند.
